2023年11月22日,来自北京生命科学研究所邵峰团队等在《自然》杂志上发表了标题为“Recognition and maturation of IL-18 by caspase-4 noncanonical inflammasome.”的研究成果,提出了Caspase-4 非典型炎症小体对IL-18的识别和成熟机制。
据介绍,经典的(caspase-1)和非经典的(包括caspase 4、5和11;以下称为caspase 4/5/11)炎症小体都切割gasdermin D(GSDMD)以诱导细胞焦亡。虽然caspase-1处理IL-1β和IL-18以实现成熟,但脂多糖激活的caspase-4/5/11尚未确定细胞因子靶标。
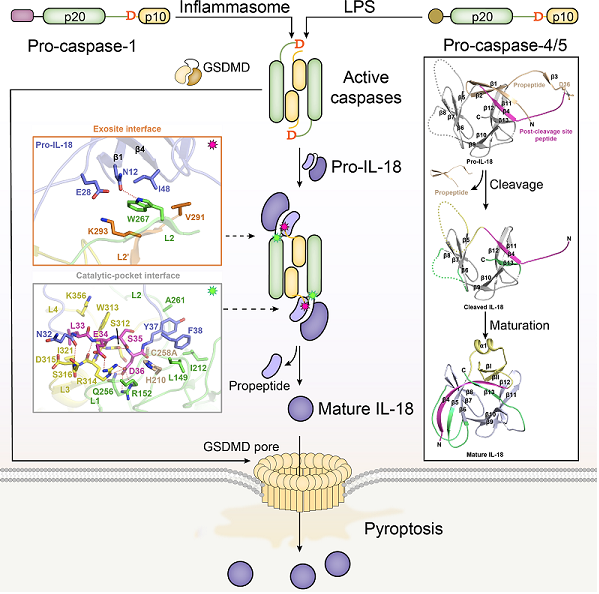
天然免疫炎症小体通路中caspases识别和活化炎症因子IL-18的示意图
研究人员发现激活的人caspase-4,而不是小鼠caspase-11,在体外和细菌感染期间直接有效地处理IL-18。caspase-4-pro-IL-18配合物的晶体结构揭示了一个二元底物识别机制;催化袋与四肽结合,并且一种独特的外源位点可以对GSDMD进行批判性识别,类似地与pro-IL-18中由前肽和后切割位点序列共同形成的特定结构结合。这种二元识别也被caspase-5和caspase-1用于处理pro-IL-18。在caspase-11中,外泌体周围的结构偏差是其无法靶向pro-IL-18的原因,而pro-IL-1是通过合理设计的突变恢复的。pro-IL-18的结构具有前肽和切割后位点区域之间的自身抑制性相互作用,阻止IL-18Rα受体的识别。caspase-1、-4或-5的切割会导致IL-18的构象发生实质性变化,从而产生两个关键的受体结合位点。
总之,这一研究发现确定IL-18是脂多糖激活的caspase-4/5的靶标。这一发现改变了对非经典炎症小体介导的防御以及IL-18在免疫和疾病中的功能理解。即发现并证明了炎症因子IL-18是非经典炎症小体通路活化的caspase-4/5的生理底物,并完整地揭示了天然免疫通路中caspases识别和切割Pro-IL-18,以及Pro-IL-18被加工后成熟为有生理功能的炎症因子的精确分子机制。成熟的IL-18重要的生理功能是诱导INFγ的产生、促进Th1型细胞免疫,非经典炎症小体通路识别和活化炎症因子IL-18的发现,为天然免疫和适应性免疫的对话提供了全新的认知。临床上,血液中高水平的IL-18与多种自身免疫疾病相关,如特异性皮炎、炎症性肠病和幼年特发性关节炎。这一成果为探索这些自身免疫疾病的发生机制以及开发新的干预策略提供了全新思路。
文章来源:
Shi, Xuyan, Sun, Qichao, Hou, Yanjie et al, Recognition and maturation of IL-18 by caspase-4 noncanonical inflammasome.DOI: 10.1038/s41586-023-06742-w, Nature:最新IF:69.504

微信扫码在线客服