近年来,开发蛋白靶向降解技术成为药物研发新的热门方向。蛋白降解技术的研究使得许多已知的不可成药靶点成为可成药靶点,并有望克服耐药性问题。蛋白靶向降解技术的研究主要是用于去除特定肿瘤蛋白,在自身免疫疾病等治疗方面的研究也取得了较大的突破。
如何通过作用于绝大多数的不可成药靶点来开发药物成为许多公司的研发重点,当前研究最多的是利用核酸药物或基因治疗的手段,对这些靶点的基因水平进行控制,以达到控制靶点蛋白水平的目的。
细胞内蛋白降解途径主要有溶酶体途径和泛素-蛋白酶体系统(ubiquitin - proteasome system , UPS)。其中,泛素-蛋白酶体系统是体内蛋白降解的主要途径,体内80%的蛋白通过该途径降解。因此,蛋白降解技术相关的研究也主要围绕此途径开展,相关项目进展也更快。
蛋白靶向降解(TPD)技术不仅可以靶向传统意义上不可成药的蛋白,而且相比于蛋白活性抑制剂可以更为彻底地阻断靶蛋白的生物功能,是近年来药物研发的热点。目前TPD蛋白降解剂主要依赖泛素-蛋白酶体(如蛋白水解靶向嵌合体PROTACs)或者溶酶体(如溶酶体靶向嵌合体LYTACs),而这两者是真核细胞有膜细胞器(如线粒体、叶绿体、过氧化物酶体等)内所不具备的。因此目前已有的蛋白靶向降解技术对于有膜细胞器内特定蛋白的降解无能为力。近日,中科院杭州医学所的方晓红团队利用线粒体基质中丰富的AAA+蛋白水解酶,发展了一种具有普适性、可模块化设计的线粒体基质蛋白靶向降解新方法。
线粒体被称为细胞的能量工厂,至今已在线粒体中发现1000多种蛋白质,广泛参与细胞的生长、运动、应激响应等生物学过程。线粒体蛋白的异常是诸如神经退行性疾病、肿瘤等恶性疾病的重要驱动因素。靶向调控线粒体基质蛋白的稳定性及降解在疾病治疗和药物开发中具有重要价值。虽然线粒体基质不具有泛素-蛋白酶体或者溶酶体,但是富集了多种由细胞核基因编码的AAA+蛋白酶(如ClpP、LONP1等)。线粒体内部主要通过这些AAA+蛋白酶对靶蛋白进行水解切割,以精确控制线粒体的蛋白稳态。同时在细胞应激状态下,胞浆中大量变性蛋白质被也会被转运到线粒体基质中,经由AAA+蛋白酶进行快速降解。以上特性提示可利用这一类AAA+蛋白酶发展线粒体基质蛋白适用的靶向降解技术。
在针对肿瘤标志物的前期研究中,科技部纳米重大科学研究计划项目首席科学家(2007-2017)方晓红教授团队,在针对肿瘤标志物的前期研究中,通过发展核酸适体技术、高通量蛋白抑制剂筛选技术等,发现可以通过小分子化合物诱导线粒体基质蛋白经由AAA+蛋白酶快速降解,证明了利用AAA+蛋白酶来靶向降解线粒体基质蛋白的可行性(J. Am. Chem. Soc., 2019, 141, 18492-18499)。然而上述线粒体基质蛋白小分子降解剂需要针对不同蛋白进行个性化的高通量筛选才能获得,开发更为普适性的、可模块化设计的线粒体基质蛋白降解新方法具有重要意义。
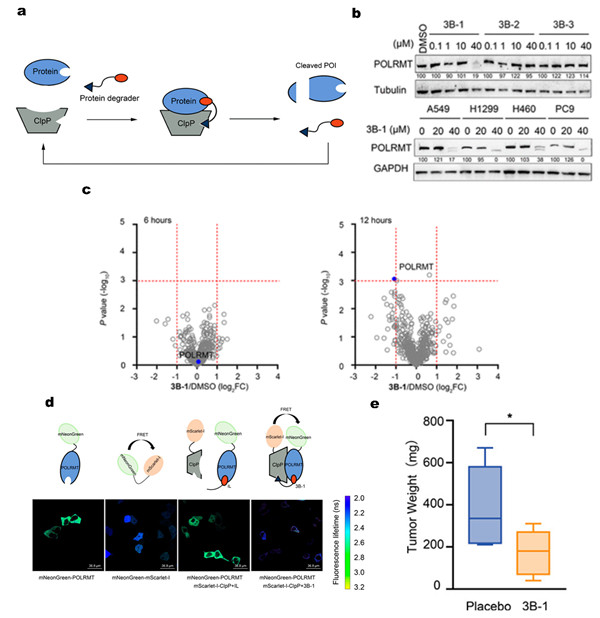
研究团队借鉴经典的PROTAC分子结构,设计了能够诱导线粒体基质靶蛋白与AAA+蛋白酶相互作用并高效水解的线粒体蛋白酶靶向嵌合体MtPTAC。以AAA+蛋白酶中水解能力最强的ClpP为蛋白降解机器,以定位于线粒体内并具有促进肿瘤生长功能的线粒体RNA聚合酶POLRMT为靶蛋白,合成了由聚乙二醇PEG链连接ClpP和POLRMT配体的MtPTAC分子。利用多种细胞系证实了设计合成的MtPTAC分子具备强大的线粒体基质靶蛋白降解能力。进一步表征分析了MtPTAC的浓度、时间以及PEG链长对靶蛋白切割降解效率的影响。通过细胞FRET成像、分子动力学模拟等探究了MtPTAC降解靶蛋白的分子机制,证实合理设计的MtPTAC分子可以拉近靶蛋白POLRMT与AAA+蛋白酶ClpP的空间距离,并触发ClpP依赖性的POLRMT水解。高通量蛋白组学实验结果表明这种水解具有较好的特异性,对线粒体其他蛋白的表达量影响小。最后通过体外细胞实验与小鼠体内成瘤实验,证实MtPTAC分子在体内可通过对靶蛋白的切割降解展示出比单独使用靶蛋白活性抑制剂更强的抗肿瘤能力。
线粒体基质蛋白靶向降解MtPTAC技术为线粒体相关疾病的治疗提供了新思路。值得注意的是,过去报道的蛋白降解剂只是拉近了靶蛋白与蛋白降解器之间的空间距离,而MtPTAC中使用的AAA+蛋白酶结合配体还可直接增强其水解酶活性,是首个结合-激活型小分子降解剂。综上,该工作发展了一种新的细胞器靶蛋白降解技术,为TPD提供了一个新的平台策略。
上述研究工作近期发表于J. Am. Chem. Soc.上,第一作者为中科院杭州医学所博士生王大驰(与中国科学技术大学联合培养)和博士后王文溪,通讯作者为中科院杭州医学所单分子生物医学研究团队的方晓红研究员和周卫副研究员。本工作得到了国家重点研发计划、国家自然科学基金委以及浙江省自然科学基金项目的资助。
文献参考:
Mitochondrial Protease Targeting Chimeras for Mitochondrial Matrix Protein Degradation
Dachi Wang, Wenxi Wang, Le Fang, Lubin Qi, Yuchao Zhang, Jie Liu, Yuxin Liang, Hongwei Yang, Mengjie Wang, Xiaojian Wei, Ruibin Jiang, Yuan Liu, Wei Zhou*, and Xiaohong Fang*
J. Am. Chem. Soc., 2023, DOI: 10.1021/jacs.3c03756

微信扫码在线客服