胞葬作用 (Efferocytosis),即吞噬细胞对凋亡细胞的吞噬,相信大家都有了解过,今天通过了解胞葬作用中嗅觉阶段、吞噬阶段、消化阶段。各阶段的关键信号分子和相关信号通路可作为治疗胞葬异常性疾病的药物开发靶点,今天让我们通过一篇发表于Nat Rev Drug Discov(IF:112.228)题为“Drugging the efferocytosis process: concepts and opportunities”的综述文章,一探究竟。

人体每天大约有200-3000亿个细胞主要通过半胱天冬酶依赖性细胞凋亡的死亡过程被更新,对于机体各种组织中的组织稳态、胚胎发育、伤口愈合和炎症消退至关重要。细胞死亡与凋亡细胞的高效吞噬作用高度结合,导致凋亡细胞很难被观察到。而凋亡细胞清除失败或缺陷可能会导致多种病理状况,这也为靶向胞葬作用过程的各个步骤发挥抗炎作用提供可能。
胞葬作用有两个好处:
一是快速去除凋亡细胞可防止它们继发坏死,在那里它们可能会释放诱发炎症的潜在毒性细胞内物质;
二是吞噬细胞通过增加抗炎介质的分泌和上调促修复转录程序,转变为更“促分辨率”的表型,使得体内数十亿死亡细胞以一种避免炎症和非免疫原性的方式被清除。
胞葬作用步骤及治疗前景
胞葬受多因素影响,多个步骤参与其中,包括“嗅觉阶段”,在此期间吞噬细胞“感知”凋亡细胞的存在并定位它们。其次是“进食阶段”,此时凋亡细胞上的配体与吞噬细胞上的吞噬细胞受体结合,特异性识别和摄取垂死的细胞。第三是“消化阶段”,处理摄入死亡细胞及其内容物。
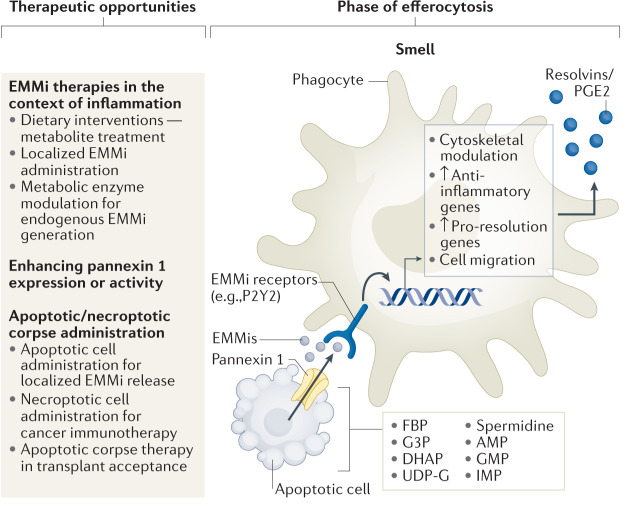
嗅觉阶段
“find me”信号:
凋亡细胞:核苷酸(ATP、UTP)、LPC、S1P、CX3CL1
吞噬细胞:G2A、CX3CR1、LRP1、SRB1、P2Y2
凋亡细胞释放可溶性介质,包括多个“识我”信号,具有双重作用,一方面作为吞噬细胞向凋亡细胞迁移的吸引信号;另一方面通过调节吞噬细胞骨架,增强吞噬受体的表达,为吞噬做准备(图1)。
少量凋亡细胞内核苷酸(<1%)的调节释放可以作为单核细胞/巨噬细胞向凋亡细胞迁移的有效诱导剂,并促进组织附近的抗炎基质。最近研究表明,pannexin 通道介导T细胞释放ATP和AMP,随后转化为腺苷,可以抑制气道炎症。凋亡细胞在凋亡早期主动释放>100种代谢物,这些代谢物作为准备信号反过来诱导吞噬细胞和邻近细胞的转录变化,被鉴定为诱导与炎症消退和组织修复相关的基因表达。
治疗前景:代谢物中的一小部分可以被用作“药物”来诱导促修复和抗炎基因转录程序。通过pannexin通道促进AMP、其他核苷酸或代谢物的调节释放是一种潜在的药物靶向策略,如“体外光分离疗法”(ECP)用于抑制系统性红斑狼疮(SLE)和关节炎的炎症以及移植排斥反应;暴露于供体凋亡细胞的移植小鼠的排异反应大大降低。
进食阶段
“eat me”信号:
凋亡细胞:PtdSer(PS)、氧化磷脂、内质网驻留钙蛋白
吞噬细胞受体:TAM(Axl、Tyro3、MerTK)、TIM、TG2
“don't eat me”信号:
凋亡细胞:CD47、CD31
吞噬细胞受体:SIRPα
桥接分子:MFGE8、GAS6、ProS、血清补体C1q、Thbs1、AnxⅠ
凋亡细胞表面“吃我”信号被吞噬细胞特异性受体识别,触发一系列复杂的细胞骨架重排,从而促进细胞吞噬“废物”,如吞噬细胞直接或间接识别凋亡细胞的磷脂酰丝氨酸(PS)受体。细胞上暴露“不要吃我”信号有助于避免细胞吞噬,现已经发现多种“不要吃我”分子,包括CD47和CD24(图2)。
治疗前景:多样性PS受体参与多种病理过程,使其成为有吸引力的治疗靶点。PS受体信号传导的小分子抑制剂作为癌症治疗药物正处于临床试验的后期阶段。CD47与巨噬细胞上的SIRPα结合,通过募集SHP1/2抑制非肌肉肌球蛋白IIA来抑制吞噬作用,可依此作为抗癌免疫新疗法的探索。单克隆抗体阻断CD24–Siglec10(肿瘤相关巨噬细胞上的唾液酸结合免疫球蛋白样lection 10)相互作用可以增加对肿瘤细胞的吞噬。

消化阶段
在细胞吞噬期间,细胞内区室之间和细胞外空间的代谢物转移可以改善抗炎基因表达和细胞吞噬的维持。吞噬细胞合成和分泌特殊的促溶解介质(SPM)是调节细胞吞噬作用抗炎功能的另一途径。吞噬细胞需要管理其体积和表面积来“包容”摄入“货物”的多少,且摄入的“货物”含有膜、胆固醇、蛋白质、核酸等,这些高代谢负担需要被代谢、被排泄或重新进入吞噬细胞的代谢通量循环。最近的研究还表明,吞噬细胞内的线粒体动力学可能在调节其体内平衡和连续性中发挥重要作用(图3、4)。
治疗前景:人类慢性肉芽肿病患者单核细胞的PPARγ已被证明可以促进胞吐作用(通过增加PS受体表达)并诱导抗炎基因表达;吞噬细胞的连续吞噬作用受阻时,增强SLC家族成员或溶酶体精氨酸转运蛋白Pqlc2活性,可以在体外和体内驱动持续的吞噬作用。利用细胞凋亡“货物”的摄入触发代谢重编程,帮助吞噬细胞抑制炎症信号的特点,将免疫行为与代谢通量联系起来的复杂蛋白质相互作用网络已成为高度优先的药物靶点。


胞葬作用涉及高度组织特异性PS受体和凋亡细胞负荷,是细胞更新普遍存在的现象。靶向胞葬药物已逐渐走进医学研究者视野,在炎症、动脉粥样硬化、糖尿病以及衰老中具有极大的治疗潜力。然而明确靶向疾病相关组织细胞受体以及冗杂的转运蛋白体系是一个极大挑战,如癌症中胞葬的“正常”作用、结核分枝杆菌感染后胞葬的细菌传播等均限制了靶向治疗的进展。这需要多学科组合研究胞葬作用的动态过程,提高靶向胞葬作用药物联合治疗相关疾病的可能性。
参考文献:Mehrotra P, Ravichandran KS. Drugging the efferocytosis process: concepts and opportunities. Nat Rev Drug Discov. 21(8), 601-620 (2022).
下一篇:蛋白质印迹手册之二蛋白质结合

微信扫码在线客服