补体系统(Complement system)是免疫系统的一个关键部分,由一组共同工作以保护身体免受感染并支持免疫反应的蛋白质组成。它在识别和消除病原体、促进炎症以及促进细胞碎片清除中起着至关重要的作用。对补体系统的研究至关重要,首先,它有助于理解其与免疫系统其他组成部分的复杂相互作用,揭示免疫反应背后的机制。其次,研究补体系统有助于为各种免疫相关疾病和自身免疫疾病开发治疗策略。特别是在Eculizumab和C1-INH成功引入之后,更多的补体基础治疗药物已经获得批准进入临床试验或使用。对补体系统的全面研究有助于推进免疫学的发展,为改善治疗和预防一系列健康状况铺平了道路。
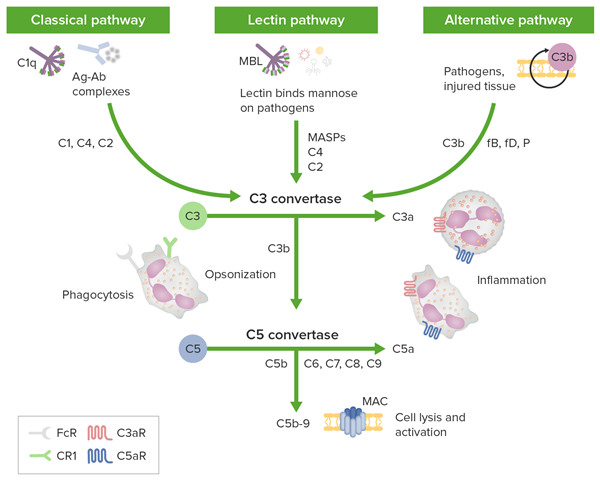
补体系统可通过三条既独立又交叉的途径被激活,即经典途径(classical pathway)、凝集素/MBL途径(lectin pathway)和旁路途径(alternative pathway,也叫替代途径)。
WIESLAB 功能性补体测定试剂盒是Svar Life Science提供的补体研究工具,它通过快速的基于ELISA的分析准确描述补体系统的三条途径(经典途径,凝集素途径,旁路途径)。这些试剂盒助力于特定途径的功能分析,而不会产生跨途径的干扰,使它们成为补体靶向药物开发和临床诊断中必不可少的工具。
 |  |
产品货号 | 英文名称 | 说明 |
WIESLAB Complement System Alternative Pathway 补体旁路途径ELISA检测试剂盒 | 用于人血清中功能性旁路补体途径的定性测定 | |
WIESLAB Complement System Classical Pathway 补体经典途径ELISA检测试剂盒 | 用于人血清中功能性经典补体途径的定性测定 | |
WIESLAB Complement System MBL Pathway 补体凝集素途径ELISA检测试剂盒 | 用于人血清中功能性经典补体途径的定性测定 | |
WIESLAB Complement System Screen 补体途径筛选检测试剂盒 | 用于人血清中功能性经典途径、凝集素途径和旁路途径补体系统的定性测定 |
经典途径是由抗体(IgG或者IgM)与抗原形成的复合物与C1q(级联反应的第一个蛋白)结合启动的,导致C1r的激活,进而裂解C1s。这反过来激活了丝氨酸蛋白酶,导致C4和C2的裂解,形成C4b2a(C3转化酶),进而裂解C3成C3a和C3b。C3a作为炎症细胞的招募因子(过敏毒素),而C3b则与C4b2a复合物结合形成C5转化酶(C4b2a3b)。C5转化酶启动膜攻击复合物(MAC)的形成,该复合物插入膜中,在细菌膜中形成功能性孔道,导致细菌溶解。
凝集素途径是由凝集素,甘露糖结合蛋白(MBP或血清凝集素)与入侵的外来细胞表面的甘露糖或N-乙酰葡萄糖胺残基结合而启动的。MBP在结构上与C1相似,由于其与糖残基的结合,激活了凝集素途径的第一个蛋白酶前体,即MBP相关丝氨酸蛋白酶(MASP1)。MASP1与Clr和CIs同源,能够蛋白水解激活MASP2,这是凝集素途径的第二个蛋白酶前体,与CIs相似。MASP1还可以激活C2和C4,但不是直接激活,而是在MASP-2的参与下进行。
C2和C4的激活产生了C3转化酶,并通过经典途径相同的反应顺序,导致MAC(膜攻击复合物)的形成。
旁路途径的激活不需要抗体或免疫复合物,而是由任何外来表面激活,如真菌、细菌多糖、脂多糖(LPSs)、颗粒和生物材料表面。通过旁路途径的补体激活在低速率下自发发生。C3内部硫酯基团在流体相中发生自发水解,生成C3·H2O。这种水解后的C3可以结合并激活因子B,并裂解另一个C3分子成C3a和C3b。在外来表面存在的情况下,C3b可能通过其硫酯结合位点的羰基与表面的羟基或氨基发生共价结合。C3b附着在表面有利于因子B和因子D与C3b的结合。因子D将因子B裂解成Ba和Bb,再次形成旁路途径的C3转化酶,C3bBb。这种附着的C3转化酶能够产生更多的C3b,导致正反馈放大循环。properdin(P因子)作用于稳定C3转化酶。C3b在表面的聚集允许形成旁路途径的C5转化酶,C3bBbC3b,并且可以裂解C5。随后TCC(膜攻击复合物)的组装与经典途径相同。
以上三条途径形成的C5转化酶,均可将C5裂解为C5a和C5b片段,C5b在液相中与C6、C7结合形成C5b67,嵌入细胞膜疏水脂质层中,进而与C8、若干C9分子聚合,形成C5b-9复合物,即末端补体复合物(terminal complement complex,TCC)。TCC以两种形式存在于体内,一是结合在细胞膜上,称为膜攻击复合物(membrane attack complex,MAC),即末端补体复合物(terminal complement complex,TCC)。TCC以两种形式存在于体内,一是结合在细胞膜上,称为膜攻击复合物,另一种是游离在血浆中与S-蛋白结合,形成SC5b-9。
补体系统对免疫系统至关重要,由一系列蛋白质组成,帮助防御感染和促进受损细胞的清除。这一防御系统在癌症中扮演着重要角色。虽然补体激活可以导致肿瘤细胞死亡,但补体和补体肽(过敏毒素)引起的慢性炎症可能是促肿瘤的,促进癌症生长。补体在肿瘤微环境中这种复杂且矛盾的作用给充分利用其在癌症治疗中的潜力带来了挑战。已经变得明显的是,补体在癌症中的作用高度依赖于特定的癌症类型和治疗策略。理解补体的多种状态和功能对于理解其在癌症进展和临床结果中的复杂作用至关重要。

微信扫码在线客服