研究目的:
Wieslab 补体系统筛选试剂盒是一种酶免疫测定法,用于定性测定人血清中功能性经典、MBL和替代补体途径,其结果不得用于临床诊断或患者管理。
补体活性受损会导致人类易患重复性暴发性或严重感染,并可能促进自身免疫疾病的发展。补体的不适当激活会导致慢性炎症和组织损伤。
艾美捷补体系统筛选试剂盒(WIESLAB Complement System Screen)(#COMPL300)的测定原理:
Wieslab 补体测定结合了补体激活的溶血测定原理和使用特定于补体激活产生的新抗原的标记抗体。产生的新抗原量与补体途径的功能活性成正比。
微孔板条的孔被经典途径、MBL途径或替代途径的特定激活剂包被。受试者血清在含有特定阻断剂的稀释液中稀释,以确保只有相应的途径被激活。在孔中孵育稀释的受试者血清期间,补体通过特定包被被激活。
然后洗涤孔,并使用特定的碱性磷酸酶标记抗体检测在MAC(膜攻击复合物)形成期间表达的新抗原上的C5b-9。
在进一步洗涤步骤后,通过与碱性磷酸酶底物溶液孵育获得特定抗体的检测。补体激活量与颜色强度相关,并以吸光度(光密度(OD))来衡量。
试剂盒组件和试剂储存:
一个框架,带有分离孔(4x8x3),密封在带有干燥剂的铝箔包装中。4条蓝色经典途径(CP)条带,涂有人类IgM。4条绿色MBL途径(MP)条带,涂有甘露糖。4条无色替代途径(AP)条带,涂有LPS。
10毫升CP稀释液(Dil CP),标为蓝色。
10毫升MP稀释液(Dil MP),标为绿色。
10毫升AP稀释液(Dil AP),标为红色。
13毫升含有碱性磷酸酶标记的C5b-9抗体的结合物(蓝色)。
13毫升即用型底物溶液。
30毫升30倍浓缩的洗涤溶液。
0.2毫升阴性对照(NC),含有人血清(应按受试者血清样本稀释)。
0.2毫升阳性对照(PC),含有冻干人血清,见下文“阳性对照的重组”。
试剂盒中的所有试剂都已准备好使用,除了洗涤溶液和对照品。试剂应储存在2-8°C,除了阳性对照。阳性对照应储存在-20°C。
所需但未提供的物料或设备:
带有405纳米滤光片的微孔板读取器。
带有一次性吸头的精密移液器。
用于条带的清洗器、吸水纸、管子和一个计时器。
结果计算:
从NC、PC和样本中减去空白(稀释液)(每个途径)的吸光度。
阳性对照的吸光度应大于1,阴性对照的吸光度应小于0.2。
阴性和阳性对照可以以半定量的方式用来计算补体活性。计算样本、PC和NC的平均OD405nm值,并按以下方式计算%补体活性:(样本-NC)/(PC-NC)x100。阴性和阳性对照旨在监测试剂的显著失败。阳性对照不能确保在测定截止值处的精确度。建议每个实验室建立自己的参考水平和缺陷的截止值。
阴性结果,即缺陷,应始终通过测试新样本来验证,以确保没有发生体外补体激活。
受试者结果:
体外补体序列的激活导致补体成分的消耗,这反过来导致它们浓度的降低。因此,补体蛋白或补体活性的测定用于指示补体系统是否已被免疫和/或病理机制激活。当怀疑补体激活性疾病或可能存在遗传性缺陷时,功能性和免疫化学补体测量都用于评估患者。通过功能性测定(如Wieslab 补体试剂盒)评估的补体活性水平考虑了成分的合成、降解和消耗速率,并提供了途径完整性的度量,与免疫化学方法相对,后者专门测量各种补体成分的浓度。当发现补体成分或补体功能水平降低时,临床医生会考虑缺陷或正在进行的免疫过程,导致成分分解增加和补体水平降低。补体水平的增加通常是急性期反应的非特异性表现。
三种Wieslab 补体测定的组合可以帮助检测补体缺陷,如下表所示:
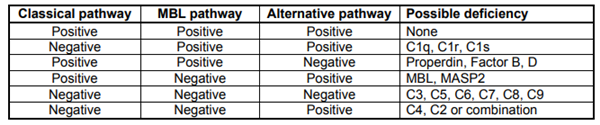
补体系统筛选试剂盒文献参考:
Walport M, Complement (First of two parts) N Engl J Med 2001, 344, 1058-1066.
Walport M, Complement (Second of two parts) N Engl J Med 2001, 344, 1140-1144.
Roos A, Bouwman L, Munoz J et al. , Functional characterization of the lectin pathway of complement
in human serum. Mol Immunol 2003, 39, 655-668.
Nordin Frediksson G, Truedsson L, Sj?holm A. New procedure for detection of complement deficiency
by ELISA. J Imm Meth 1993, 166, 263-270.

微信扫码在线客服