癌症是发达国家妇女中最常见的危及生命的恶性病变如今,每年约有18万例新确诊病例。其中大约一半是新的确诊的患者是淋巴结阴性,但这些病例中有30%进展为转移性疾病。有许多肿瘤标志物可以帮助临床医生识别和诊断哪种乳腺癌症患者将患上更具侵袭性的疾病。这些标志物包括雌激素和黄体酮受体、DNA倍体和S期百分比、表皮生长因子受体、HER-2/neu癌基因、p53抑癌基因、组织蛋白酶D、增殖标志物和CA15-3。CA15-3最多可用于监测患者术后复发,特别是在转移性疾病病例中。96%的局部和全身复发患者CA15-3升高,可用于预测复发早于放射学和临床标准。血清CA15-3增加25%与随着癌症的进展。血清CA15-3下降50%与对治疗。CA15-3在乳腺癌症复发早期检测中比CEA更敏感。联合CA125、CA15-3已被证明可用于早期检测卵巢癌复发癌症CA15-3水平在结肠、肺和肝肿瘤中也升高。
Calbiotech-CA15-3 ELISA试剂盒用于定量测定人血清或血浆中癌症抗原CA15-3的浓度。
艾美捷Calbiotech-CA15-3 (Cancer antigen 15-3) ELISA Kit:
目录编号:CA240T
产品类型:ELISA
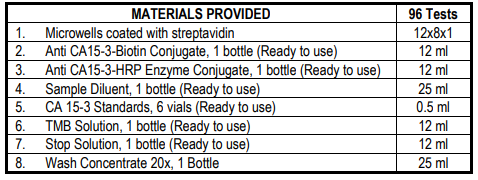
数量:96次测试(12x8易碎条状井)
标准范围:10-240 U/mL
样本体积:25 微升/孔
物种:人类
储存和稳定性:将试剂盒存放在2-8°C的环境下。确保微孔板密封在装有干燥剂的干燥袋中。试剂在试剂盒有效期内保持稳定。不要将测试试剂暴露在热源、阳光或强光下。
CA15-3 (Cancer antigen 15-3) ELISA Kit检测原理:
CA15-3 ELISA检测是一种改良的固相序贯夹心ELISA。将样品和生物素化单克隆抗体加入涂有链霉抗生物素蛋白的孔中。患者样本中的CA15-3与生物素化捕获抗体结合。生物素化抗体同时与链霉抗生物素蛋白包被板结合。洗涤步骤后,加入抗CA15-3-HRP酶偶联物,并在捕获的CA15-3周围形成三明治。未结合的抗体被洗掉。加入TMB底物导致蓝色的发展。CA15-3的浓度与产生的颜色强度成正比。生成颜色强度与CA15-3浓度相关的标准曲线。
测定程序:
将所有样本和试剂盒组分置于室温(20-25°C)下,并轻轻混合。
1. 使用前应将患者样本稀释10倍。(见上述试剂和样本准备)不要稀释标准品。
2. 在架中固定所需数量的包被孔。向相应的孔中分配25微升的CA15-3标准品、稀释样本和稀释对照品。
3. 向所有孔中加入100微升的抗体-生物素结合试剂(蓝色溶液)。轻轻混合20-30秒,转速为500-600转/分钟。
4. 在室温下孵育60分钟。
5. 从所有孔中移除液体。用350微升的1X洗涤缓冲液洗涤每个孔三次。每次洗涤后,将板倒置在吸收纸上或纸巾上,用力敲击以去除残留液滴。
6. 向每个孔中分配100微升的酶结合物(红色溶液)。
7. 在室温下孵育60分钟。
8. 按照上述第5步的描述,移除内容物并洗涤板3次。
9. 向每个孔中分配100微升的TMB溶液。
10. 在室温下孵育15分钟。
11. 通过向每个孔中加入50微升的终止液来终止反应。
12. 在15分钟内使用微孔板读取器在450nm处读取吸光度(使用630nm的参考波长)。
Calbiotech-CA15-3 (Cancer antigen 15-3) ELISA Kit文献参考:
Aziz DC, Peter JB. DNA ploidy and cell-cycle analysis. Tools for assessment of cancer prognosis. J Clin Pathol 1991;5:422-38.
Clark GM, Dressler LG, Owens MA, Dounds G, Oldaker T, McGuire WL. Prediction of relapse or survival in patients with node-negative breast cancer by DNA flow cytometry. N Engl J Med 1989;320:627-33.
Elledge RM, McGuire WL. Prognostic factors and therapeutic decisions in axillary node-negative breast cancer. Annu Rev Med 1993;44:201-10.
Foekens JA, Rio C, Seguin P, et al. Prediction of relapse and survival in breast cancer patients by pS2 protein. Cancer Res 1990; 50-3832-7.
Isola J, Visakorp T, Holli K, Kallionieml D. Association of p53 expression with other prognostic factors and long term survival in node-negative breast cancer. J Cell Biochem 1992;(Suppl 16D):101.
Kute TE, Shao ZM, Snugg NK, Long RT, Russell GB, Case LD. Cathepsin D as a prognostic indicator for node-negative breast cancer patients using both immunoassays and enzymatic assays. Cancer Res 1992;52-198-203.
McGuire WL, Tandon AK, Allred D, Chamnes GC, Clark GM. How to use prognostic factors in axillary node negative breast cancer patients. J Natl Cancer Inst 1990;82:1006-7.
Nicholson S, Richard J, Sainsbury C, et al. Epidermal growth factor receptor (EGFr): results of a 6 year follow up study in operable breast cancer with emphasis on the node-negative subgroup. Br J Cancer 1991;63:146-50.
Somerville JE, Clarke LA, Biggart JD. C-erb B-2 overexpression and histological type of in-situ and invasive breast carcinoma. J Clin Pathol 1992;45-16-20.
艾美捷科技是Calbiotech的中国代理商,为科研工作者提供优质的产品与服务。

微信扫码在线客服