孕烯醇酮(3β-羟基孕甾-5-烯20-酮)是第1种在甾体生成过程中从胆固醇中衍生出来的类固醇,也是所有肾上腺和性腺类固醇的常见前体。通过P-450SCC酶切割胆固醇的C-20侧链,在线粒体中产生胆固醇。生产后,孕烯醇酮可通过两种甾体生成途径利用。孕烯醇酮可以通过17α-羟化酶的酶作用转化为17-OH孕烯醇酮,也可以通过3β-羟基类固醇脱氢酶的酶作用转变为孕酮。孕烯醇酮水平升高以先天性肾上腺增生(CAH)的形式出现,这是由于3β-羟基甾体氢化酶缺乏或17α-羟化酶缺乏所致。据报道,特发性多毛症妇女的水平也较高。关于性别和年龄差异的孕烯醇酮水平研究表明,女性和男性的最高水平分别出现在17岁和16岁左右,而女性和男性分别出现在37岁和38岁左右。一般来说,与男性相比,女性的价值略高。孕烯醇酮生理学的许多领域仍有待研究。目前的研究表明,血清中孕烯醇酮的测定可能有助于研究其代谢产物硫酸孕烯醇酮,据报道,硫酸孕烯醇在哺乳动物大脑和中枢神经系统中具有多种作用。
艾美捷Biogradetech-人孕烯醇酮ELISA Kit(BGT-KET-150)人孕烯醇酮 ELISA Kit预期用途:
用于人血清中孕烯醇酮的直接定量测定,采用酶免疫分析法。仅限于体外诊断使用。
人孕烯醇酮ELISA Kit检测原理:
以下酶免疫分析检测的原理遵循典型的竞争性结合场景。未标记的抗原(存在于标准品、对照品和患者样本中)与酶标记的抗原(结合物)在微孔板上有限数量的抗体结合位点之间发生竞争。洗涤和倒液步骤去除未结合的物质。洗涤步骤后,加入酶底物。酶促反应通过加入终止液来终止。在微孔板阅读器上测量吸光度。形成的色泽强度与样本中孕烯醇酮的浓度成反比。使用一组标准品绘制标准曲线,从而可以直接读取患者样本和对照品中孕烯醇酮的浓度。
操作注意事项和警告:
1. 用户应彻底理解本协议,以成功使用此试剂盒。只有通过严格遵守和仔细遵循所提供的说明,才能获得可靠的性能。
2. 建议所有客户准备自己的控制材料或血清池,应在每次运行中包含高浓度和低浓度水平,以评估结果的可靠性。
3. 当指定使用水进行稀释或重悬时,请使用去离子水或蒸馏水。
4. 为了减少接触潜在有害物质的风险,处理试剂盒试剂和人类样本时应佩戴手套。
5. 所有试剂盒试剂和样本在使用前应放置至室温,并轻轻但彻底地混合。避免试剂和样本反复冻融。
6. 每次运行时都必须建立标准曲线。
7. 试剂盒中提供的对照品应包含在每次运行中,并且必须落在既定的置信限内。
8. 如果对照品的检测值没有反映出既定范围,可能表明操作程序不当、移液不精确、洗涤不完全或试剂储存不当。
9. 读取微孔板时,孔中的气泡会影响光密度(OD)。在执行读取步骤之前,仔细去除任何气泡。
10. 底物溶液(TMB)对光敏感,如果储存得当,应保持无色。出现蓝色表示不稳定或受污染,此时不应使用。
11. 分装底物和终止液时,不要使用这些液体会接触到任何金属部件的移液管。
12. 为了防止试剂污染,分装每个试剂、样本、标准品和对照品时,使用新的一次性移液管尖。
13. 不要在测试中混合不同批号的试剂盒组分,并且不要使用任何超出标签上打印的有效期的组分。
14. 试剂盒试剂必须被视为危险废物,并根据国家规定进行处置。
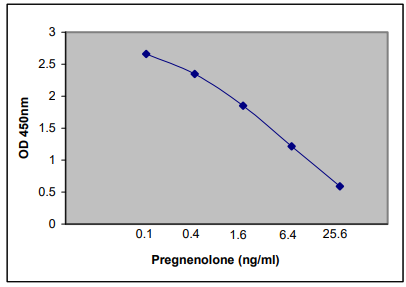
仅对曲线进行采样。不要使用来计算结果。
人孕烯醇酮ELISA Kit文献参考:
1. Abraham GE, et al. Radioimmunoassay of Plasma Pregnenolone, 17-hydroxy-pregnenolone and Dehydroepiandrosterone Under Various Physiological Conditions. J Clin Endocrinol Metab. 1973; 37(1):140–4.
2. Hill M, et al. Age Relationships and Sex Differences in Serum Levels of Pregnenolone and 17-hydroxypregnenolone in Healthy Subjects; Clin Chem Lab Med. 1999; 37(4):439–47.
3. Robel P, et al. Biosynthesis and Assay of Neurosteroids in Rats and Mice. J Steroid Biochem Mol Biol.1995; 53:355–60.
4. Weusten JJ, et al. Early Time Sequence in Pregnenolone Metabolism to Testosterone in Homogenates ofHuman and Rat Testis. Endocrinlogy. 1987; 120(5):1909–13.
5. Akwa Y, et al. Neurosteroids: Biosynthesis, Metabolism and Function of Pregnenolone andDehydroepiandrosterone in the brain. J Steroid Biochem Mol Biol. 1991; 40(1-3):71–81.
6. McKenna TJ, Brown RD. Pregnenolone in Man: Plasma Levels in States of Normal and AbnormalSteroidogenesis. J Clin Endocrinol Metab. 1974; 38(3):480–5.
7. McKenna TJ, et al. Pregnenolone, 17-OH-Pregnenolone, and Testosterone in Plasma of Patients withCongenital Adrenal Hyperplasia. J Clin Endocrinol Metab. 1976; 42(5):918–25.
8. McKenna TJ, et al. Plasma Pregnenolone in Patients with Adrenal Tumors, ACTH Excess, or IdiopathicHirsutism. J Clin Endocrinol Metab. 1977; 44(2):231–6.
9. Wilson JD, Foster, DW, eds. Williams Textbook of Endocrinology 8th Edition. London: W.B. SaundersCompany; 1992:495-7.
10. Check JH, et al. Falsely Elevated Steroidal Assay Levels Related to Heterophile Antibodies Against VariousAnimal Species. Gynecol Obstet Invest. 1995; 40(2):139–40.

微信扫码在线客服