乙型肝炎表面抗原或HBsAg是乙型肝炎病毒包膜中Z重要的蛋白,负责急性和慢性病毒性肝炎。表面抗原包含决定因素“a”,这是所有已知病毒亚型共有的,通过两个不同的亚组(ay和ad)在免疫学上区分。近年来,通过高灵敏度免疫分析检测HBsAg的能力,促进了对其全球分布和流行病学的理解,并从根本上降低了输血中感染的风险。
第四代酶免疫分析(ELISA)用于一步法测定人血浆和血清中的乙型肝炎表面抗原(HBsAg)。该试剂盒旨在筛查血液单位,能够检测HBsAg突变体,并在HBV感染患者的随访中得到应用。仅限于“体外”诊断使用。
艾美捷Biogradetech-HBsAg ELISA试剂盒(BGT-KET-152)检测原理:
一种针对HBsAg的“a”、“d”和“y”决定因素的特异性小鼠单克隆抗体混合物被固定在微孔板表面。将患者血清/血浆与第二种小鼠单克隆抗体混合,这些抗体与辣根过氧化物酶(HRP)结合,并且针对“a”决定因素的不同表位和“preS”。在样本中存在HBsAg时形成的特定免疫复合物被固相捕获。在一步法孵育结束时,清洗微孔板以去除未结合的血清蛋白和HRP结合物。然后加入底物/色原,并且在捕获的HBsAg免疫复合物存在的情况下,无色底物被结合的HRP结合物水解成有色最终产物。在阻断酶反应后,通过ELISA读数器测量其吸光度。颜色强度与样本中存在的HBsAg量成正比。ULTRA版本特别适用于自动化筛查,并且能够检测“s”突变体。
所需但不提供的材料:
1. 校准的微量移液管(150微升、100微升和50微升)和一次性塑料吸头。
2. EIA级水(双蒸馏或去离子,经木炭处理以去除用作消毒剂的氧化性化学物质)。
3. 具有60分钟或更长范围的定时器。
4. 吸水纸。
5. 校准的ELISA微孔板恒温孵育箱(干式或湿式),能够以1300转/分钟 +/- 150的速度提供摇晃,设定在+37°C。
6. 校准的ELISA微孔板阅读器,具有450纳米(读数)和620-630纳米(空白)滤光片。
7. 校准的ELISA微孔板洗涤器。
8. 涡旋混合器或类似的混合工具。
样本:准备和警告
1. 通过无菌静脉穿刺采集血液,并使用临床实验室分析样本的标准技术制备血浆或血清。使用柠檬酸盐、EDTA和肝素制备样本的过程中没有观察到影响。
2. 避免向样本中添加任何防腐剂;特别是亚硝酸盐,因为这种化学物质会影响结合物的酶活性,导致假阴性结果。
3. 必须用代码或名称清楚地标识样本,以避免结果解释错误。当试剂盒用于血液单位筛查时,强烈推荐使用条码标签和电子阅读。
4. 溶血(红色)和脂血(“乳状”)样本必须丢弃,因为它们可能会产生虚假结果。含有纤维蛋白残留、大颗粒或微生物丝和体的样本也应丢弃,因为它们可能会导致假阳性结果。凝血途径改变的样本,在采血和制备血清/血浆后呈现颗粒,如来自血液透析患者的样本,可能会产生假阳性结果。
5. 血清和血浆可以在+2°C至+8°C的一次性收集管中储存,自采集后最多五天。不要冷冻一次性收集管。对于更长时间的储存,仔细从一次性收集管中取出的血清和血浆样本,可以在-20°C下冷冻储存至少12个月。任何冷冻样本不应冻融超过一次,因为这样可能会产生影响测试结果的颗粒。
6. 如果解冻后存在一些混浊或怀疑存在微粒,应通过一次性0.2-0.8μm过滤器过滤样本以清洁它进行测试,或者使用两步替代方法。
结果解释:
测试结果根据以下表格,解释为样本OD450nm/620-630nm(S)与截止值(Co)的比率,用数学表示为 S/Co:
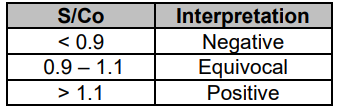
阴性结果表明患者未感染乙型肝炎病毒(HBV),因此该血液单位可以进行输血。
任何呈现不确定结果的患者应在初次样本采集后1-2周重新采集样本进行复测;该血液单位不应进行输血。
阳性结果表明存在HBV感染,因此应对患者进行相应的治疗或该血液单位应被废弃。
HBsAg ELISA试剂盒文献参考:
1. Aach R.D., Grisham J.W., Parker S.W.. Detection of Australiaantigen by radioimmunoassay. Proc.Natl.Acad.Sci..USA, 68:1956,1971.
2. Blumerg B.S., Suinick A.I., London W.T.. Hepatitis and leukemia:their relation to Australia antigen. Bull.N.Y.Acad.Med.. 44:1566,1968.
3. Boniolo A., Dovis M., Matteja R.. The use of enzyme-linkedimmunosorbent assay for screening hybridoma antibodies againsthepatitis B surface antigen. J.Immunol.Meth.. 49:1, 1982.
4. Caldwell C.W., Barpet J.T.. Enzyme immunoassay for hepatitis Band its comparison to other methods. Cli.Chim.Acta 81: 305, 1977
5. Fazekas S., De St.Groth, Scheidegger D.. production of monoclonalantibodies: strategy and tactics. J.Immunol.Meth.. 35: 1, 1980
6. Reesink H.W.. et al.. Comparison of six 3rd generation tests for thedetection of HBsAg. Vox.Sang.. 39:61, 1980
7. Rook G.A.W.. Chromogens for the enzyme-linked immunosorbentassay (ELISA) using horseradish peroxidase. Lepr.Rev. 52: 281,1981
8. Schroder J.. Monoclonal antibodies: a new tool for reasearch andimmunodiagnostic. Med.Biol.. 58: 281, 1981
9. Coleman PF, Chen YC, Mushahwar IK. Immunoassay detection ofhepatitis B surface antigen mutants. J.Med.Virol. 1999;59(1):19-24

微信扫码在线客服