胸腺基质细胞生成素(TSLP)是一种细胞因子,在过敏性疾病如哮喘和慢性阻塞性肺病(COPD)等的发病机制中起着至关重要的作用。本技术说明概述了TSLP在这些呼吸系统疾病中的作用,并讨论了其对治疗的影响。我们探讨TSLP驱动气道炎症和重塑的机制,并回顾TSLP靶向治疗哮喘和COPD管理的最新进展。
哮喘和慢性阻塞性肺疾病(COPD)都是以气流阻塞和呼吸道症状为特征的慢性呼吸系统疾病,但它们具有不同的潜在机制和临床表现。
哮喘是一种以反复发作的喘息、呼吸急促、胸闷和咳嗽为典型特征的疾病,通常发生在夜间或清晨。它主要由气道炎症和高反应性驱动,以响应各种触发因素,如过敏原,病毒感染,运动和污染物。炎症主要是嗜酸性粒细胞性的,涉及细胞因子如白细胞介素(IL)-4、IL-5和IL-13的释放,其协调免疫细胞募集、粘液分泌过多和气道平滑肌收缩。气道重塑,其特征在于结构变化,如气道壁增厚、胶原沉积和平滑肌质量增加,可随时间发生,导致持续的气流限制和症状恶化。
另一方面,COPD主要是由暴露于烟草烟雾引起的,尽管其他环境因素如生物质燃料暴露和职业污染物也可能起作用。其特征是持续和渐进的气流限制,不完全可逆。COPD包括两种主要表型:慢性支气管炎,其特征在于慢性咳嗽和痰产生,以及肺气肿,其特征在于肺实质破坏和气腔扩大。COPD的标志性病理学特征包括慢性炎症,主要是嗜酸性和巨噬细胞驱动的,导致气道壁增厚、粘液分泌过多和肺弹性回缩丧失。此外,COPD与全身性炎症和合并症(如心血管疾病、骨骼肌功能障碍和骨质疏松症)相关,这导致其显著的发病率和死亡率。
尽管有治疗方法,但许多患者继续出现不受控制的症状,这突出了对新治疗方法的需求。TSLP已成为哮喘和COPD气道炎症和重塑的关键调节因子,为治疗干预提供了有希望的靶向方法。
TSLP是一种I型细胞因子,是IL-7的副产物,可能来源于相同的祖先基因(1)。它主要由肺、皮肤和胃肠道中的上皮细胞和基质细胞产生。多种触发因素可诱导TSLP产生,包括损伤、TLR 2(Toll样受体2)、TLR 3和NOD 2的配体、蠕虫、细菌和病毒感染、蛋白酶(如胰蛋白酶和木瓜蛋白酶)以及促炎细胞因子(2)。TSLP有效地充当放大炎症防御机制的警报分子。
TSLP与由TSLPR(胸腺基质淋巴细胞生成素受体)和IL-7受体α链(IL-7 R α)组成的异二聚体受体结合,启动JAK 1和JAK 2介导的磷酸化级联反应(3)。STAT 5A和STAT 5 B的随后募集和活化最终导致Th 2相关细胞因子IL-4、IL-5、IL-9和IL-13的转录和产生。TSLPR由多种免疫细胞表达,包括T细胞、B细胞、先天性淋巴样细胞(ILC 2)、自然杀伤T(NKT)细胞、单核细胞/巨噬细胞、嗜碱性粒细胞、树突细胞(DC)以及非免疫细胞如上皮细胞、平滑肌细胞和神经细胞。
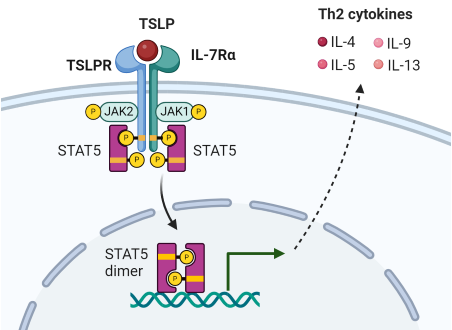

图1.通过异二聚体受体的TSLP信号传导:TSLPR和IL-7 R α。改编自Ebina-Shibuya,R.和伦纳德,WJ。2022年(1).
TSLP是由上皮细胞产生的,以响应各种触发器,如过敏原,病毒和污染物。它通过促进树突状细胞的活化和分化作为2型炎症的主要调节剂,这反过来又驱动幼稚T细胞分化为促炎性Th 2细胞。Th 2细胞因子,包括IL-4、IL-5和IL-13,协调嗜酸性粒细胞性炎症、粘液分泌过多和气道高反应性,这是哮喘的标志性特征。此外,TSLP通过促进细胞外基质蛋白的产生和成纤维细胞活化来促进气道重塑。因此,靶向TSLP信号通路有望减轻哮喘的炎症和重塑。
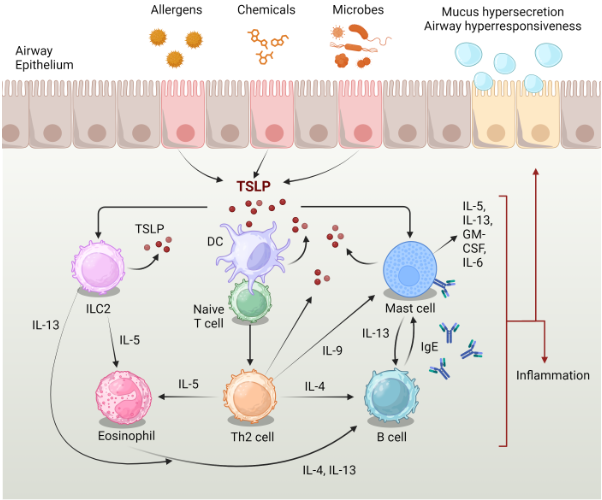
图2. TSLP驱动哮喘中的Th 2炎症通路。改编自Ebina-Shibuya,R.和伦纳德,WJ。2022年(1).
在COPD中,TSLP表达响应于香烟烟雾暴露和呼吸道感染而上调。TSLP通过募集和激活先天性免疫细胞(包括嗜中性粒细胞和巨噬细胞)导致促炎介质的产生而促成慢性炎症。此外,TSLP诱导气道平滑肌增殖和胶原沉积,有助于COPD的气流限制和肺功能下降。靶向TSLP通路为解决COPD中的炎症和重塑以及潜在地减缓疾病进展提供了一种新方法。
正在探索几种靶向TSLP的治疗策略用于治疗哮喘和COPD。针对TSLP或其受体的单克隆抗体已在临床前研究和早期临床试验中显示出疗效,证明了肺功能、症状和加重率的改善。TSLP信号通路的小分子抑制剂也在开发中,并有望作为长期疾病管理的口服疗法。靶向多种炎症通路(包括TSLP)的联合治疗可提供协同效应,并改善重度哮喘和COPD表型的治疗结局。靶向TSLP信号通路代表了这些呼吸系统疾病的有希望的治疗方法,提供了缓解症状,改善肺功能和改变疾病进展的潜力。进一步的研究是必要的,以充分阐明复杂的机制TSLP和优化的治疗策略,临床实施。
| 产品名称 | 货号 | 规格 |
TSLP应答性荧光素酶报告基因Ba/F3细胞系 TSLP Responsive Luciferase Reporter Ba/F3 Cell Line | BPS-82500 | 2 vials |
该细胞系是一种鼠Ba/F3细胞系,经工程改造可表达TSLPR和IL-7 R α(白细胞介素7受体α),二者由自切割P2 A肽分开。通过转导STAT 5荧光素酶报告基因Ba/F3细胞(#79772)来递送构建体,所述细胞表达由位于最小TATA启动子上游的STAT 5应答元件驱动的萤火虫荧光素酶报告基因。在被TSLP激活后,内源性转录因子STAT 5与应答元件结合,诱导荧光素酶报告基因的转录。已验证该细胞系对TSLP有应答。它对IL-7没有反应。 额外的功能验证证明TSLP诱导的荧光素酶活性可被抗TSLP或抗TSLPR中和抗体抑制。
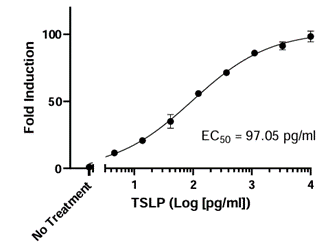

图3. TSLP响应性荧光素酶报告基因Ba/F3细胞系中对TSLP的剂量响应。


图4.抗TSLP中和抗体对TSLP应答性荧光素酶报告基因Ba/F3细胞系中TSLP应答的抑制。将TSLP响应性荧光素酶报告基因Ba/F3细胞与浓度递增的 抗TSLP中和抗体 (#102138)过夜,然后用0.3ng/ml TSLP刺激。荧光素酶活性使用 ONE-Step?荧光素酶测定系统 (#60690)。结果显示为STAT5报告子活性的百分比(与在不存在抗体的情况下由TSLP刺激的细胞相比,设定为100%)。
| 产品名称 | 货号 | 规格 |
| 抗TSLP中和抗体 Anti-TSLP Neutralizing Antibody | 102138-1 | 25 ?g |
| ONE-Step?荧光素酶测定系统 ONE-Step? Luciferase Assay System | 60690-1 | 10 ml |
为了快速筛选和验证TSLP:TSLPR相互作用的阻断剂,TSLPR:TSLP [生物素化]抑制剂筛选化学发光检测试剂盒是理想的选择。这种基于ELISA的荧光测定法提供了稳健的信噪比,并以方便的试剂盒形式提供。质量测试确保了批次间性能的一致性。


图5.抗TSLP中和抗体(#102138)对TSLP:TSLPR结合的剂量依赖性抑制。
1. Ebina-Shibuya, R. and Leonard, WJ. 2022. Nat Rev Immunol. 23:24-37. Pubmed
2. Takai, T. 2012. Allergol Int. 61:3-17. Pubmed
3. Ziegler, S. 2012. J Allergy Clin Immunol. 130:845-852. Pubmed

微信扫码在线客服