Lysophosphatidic Acid (LPA) Assay Kit II (货号EEB-K-2800S) 是一种高灵敏、特异性强、稳定性强的用于定量血浆、血清和组织匀浆中的LPA的试剂盒。
样品类型: 血清、血浆和组织匀浆(人或动物)
样品体积: 20?L/样品(重复点)
实验孵育时间: 2小时30分钟
检测范围: 0.064?M~1000?M
LPA是一种血清来源的磷脂,参与多种细胞过程,如细胞增殖、趋化性、血小板聚集、伤口愈合、血管生成、肿瘤侵袭和平滑肌收缩。近年来的研究表明,LPA可能在癌症的病理生理中发挥重要作用,并可能作为卵巢癌的生物标志物。
溶血磷脂酸(LPA)测定是一种设计用于体外测定生物样品中溶血磷脂酸(LPA)的酶联免疫吸附试验。LPA检测对LPA具有特异性,对不同的酰基链敏感。该分析是一种竞争性ELISA,其中比色信号与样品中存在的LPA的量成反比。本质上,随着LPA在测定中量的增加,比色信号减少。简单地说,科学家将他们的样品与生物素化的抗lpa抗体和样品稀释剂混合。然后他们将混合物转移到LPA涂层检测板上进行竞争结合。链亲和素hrp和比色检测用于检测结合到板上的生物素化抗lpa的量。使用已知LPA量的标准曲线来确定样品中LPA的浓度。LPA测定在450nm处读取,需要3小时运行。
在本文中,我们将介绍溶血磷脂酸(LPA)检测试剂盒II的特异性数据。该ELISA检测是与Lpath(最初的抗体开发商)合作开发验证,将用于检测其对其他类似或丰富的脂质(如磷脂酸(PA)和溶血磷脂酰胆碱(LPC))的特异性,我们将展示它如何区分各种LPA物种。
LPA分析的重要参与者
Lysophosphatidic Acid(LPA)
LPA是一种血清衍生的生物活性磷脂,参与多种细胞过程,如细胞增殖、趋化性、血小板聚集、伤口愈合、血管生成、肿瘤侵袭和平滑肌收缩。最近的研究表明,LPA可能在癌症的发展中起着至关重要的作用,并可能作为卵巢癌的有用生物标志物。根据一项利用LPA测定法的初步研究,LPA水平在子宫内膜样卵巢癌患者中明显较高。测量阴道分泌物中的LPA可能为绝经后妇女诊断子宫内膜样卵巢癌提供一种无创方法。
Lysophosphatidic (LPA) Antibody
LPA Antibody 是一种专门针对LPA的新型单克隆抗体。LPA抗体最初由Lpath获得专利并开发,旨在抑制LPA在体外和体内的作用。如本文所述,LPA抗体在竞争性ELISA检测中表现出特异性。一项利用KinExA (Kinetic Exclusion Assays)进行的研究证实,LPA抗体与所有相关LPA物种,特别是16:0和18:2 LPA具有高亲和力。此外,他们发现LPA抗体可以减少创伤性脑损伤后的病变体积和扩散,表明其具有中和炎性脂质LPA的潜力,并支持其作为LPA靶向治疗药物的使用。
Lysophosphatidic (LPA) Assay
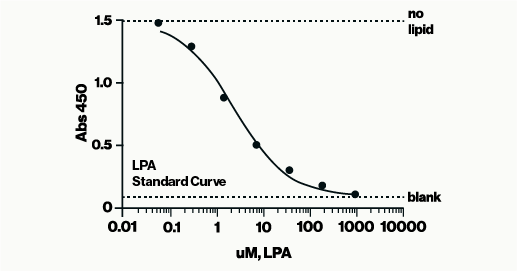
LPA Assay是一种具有竞争力的ELISA,用于测量复杂样品(如血清、血浆和组织匀浆)中的LPA水平。竞争性ELISA也称为抑制试验,通过评估分析物如何干扰分析信号来确定分析物浓度。该格式对于检测复杂混合物(包括血浆、血清或细胞提取物)中的小分析物(如脂质)特别有效,只需最少的样品处理。竞争性ELISA对样品稀释和基质效应不太敏感,并且通常在测定之间表现出较低的变化,使其成为我们许多ELISA测定的首选。
在这个实验中,含有LPA的样品与LPA抗体在样品稀释液中孵育。然后将得到的混合物涂在lpa涂层的检测板上进行竞争结合。检测采用HRP和比色法测量结合到板上的LPA抗体的量。LPA浓度是用已知LPA量的标准曲线确定的。该分析在450nm处读取,大约需要3小时才能完成。完整的协议可以在这里找到。
LPA检测对不同LPA酰基链的特异性
LPA的长度和酰基链的饱和度不同。这些差异包括链上的碳数(16-、18-或20-)以及脂肪酸是饱和的还是不饱和的。例如,16:0和18:0是饱和脂肪酸,而16:1、18:1、18:2和20:4是不饱和脂肪酸。人血清中最常见的LPA种类是18:1-LPA(油酸)、18:2-LPA(亚油酸)和20:4-LPA(花生四烯酸)。根据两份出版物(Murph2007和Sutphen2004), LPA在人血浆中的存在比例为C16:0: C18:0: C18:1: C18:2: C20:4 = 2.8:1.0:1.5:2.6:3.0。基于这些数据,我们分别测试了一个“混合LPA”和每个LPA,如下表1所示。在这个实验中,我们运行了完整的竞争曲线,并通过IC50值进行了比较。
LPA | IC50 (uM) | Ratio to C18:3 IC50 |
LPA C18:3 | 0.64 | 1 |
LPA C16:0 | 94.33 | 148 |
LPA C18:0 | 295.70 | 463 |
LPA C18:1 | 29.57 | 46 |
LPA C18:2 | 1.33 | 2 |
LPA C20:4 | 10.80 | 17 |
Mixed LPA | 1.75 | 3 |
Table 1: LPA Assay LPA acyl chain specificity
LPA酰基链特异性结果如下:
1. LPA测定采用LPA C18:3作为测定标准;
2. LPA测定识别以下LPA种类(从高到低的顺序):C18:3 > C18:2 >混合型LPA > C20:4 > C18:1 > C16:0 > C18:0;
3. 混合LPA =存在于人血浆中的LPA种类(C16:0: C18:0: C18:1: C18:2: C20:4 = 2.8:1.0:1.5:2.6:3.0);
LPA检测对其他脂质的特异性
上文描述了利用LPA抗体的竞争性分析,他们的竞争性ELISA对LPA是特异性的,不结合其他测试的脂质(表1)。他们的结果反映了我们的内部测试,并与Lpath使用可比较的竞争性ELISA方法的结果一致。
表2给出了在200 μM的LPA实验中测试的一组脂质,测试标准为LPA 18:3。结果显示极少或无交叉反应性。除了已发表的数据和我们测试的脂质外,Lpath测试的更广泛的脂质面板(未显示)显示出类似的最小交叉反应性。基本上,当在竞争性ELISA格式中使用时,LPA抗体对其靶脂质LPA表现出高特异性。
Tested Lipid | EBI Catalog # | Detected (uM) | % cross reactivity |
S1P | S-2000 | 0.04 | 0% |
Sph | S-1000 | 0.18 | 0% |
SPC | 0.08 | 0% | |
LPC 18:0 | L-1518 | 0.04 | 0% |
PS 16:0 | L-3116 | 0.13 | 0% |
PC 16:0 | L-1116 | 0.13 | 0% |
PG 16:0 | 0.01 | 0% | |
PA 16:0 | L-4116 | <0 | 0% |
PE 16:0 | L-2182 | 0.17 | 0% |
Lyso PAF | 0.04 | 0% | |
Brp-LPA | L-7416 | 0.08 | 0% |
DAG | L-0016 | 0.05 | 0% |
ether LPA 12:0 | 0.06 | 0% | |
GP | 0.05 | 0% |
Table 2: LPA Assay lipid cross reactivity
数据表明,LPA分析法与我们所测试的脂质具有<1%的交叉反应性。如果对某一特定脂质有顾虑,此处未显示的其他测试数据可应要求共享。
综上所述,Echelon的LPA Assay对于检测LPA具有高度特异性,LPA是一种具有潜在癌症生物标志物应用价值的关键脂质。该方法的广泛验证表明,它可以有效地区分LPA与类似的脂质,确保在复杂样品中准确测量LPA。该检测的高特异性和低交叉反应性使其成为研究和临床应用的可靠工具。
原文链接:https://www.echelon-inc.com/how-specific-is-the-lpa-assay-kit-ii/?mc_cid=93d09d3c99&mc_eid=1618568324

微信扫码在线客服