【前情提示】:Flipper-TR® :一种革命性的新型活细胞膜张力荧光探针,点击了解
细胞膜张力调节许多细胞过程,如胞吞,胞吐,分裂和细胞运动1-6,所有这些过程都需要重塑细胞形态,而这反过来又依赖于细胞膜变形和肌动蛋白细胞骨架重塑之间的相互作用1,3,5-9 , 本通讯主要讨论细胞运动相关的形态发生过程中Actin细胞骨架与膜张力之间的协同作用。

细胞定向运动需要在细胞的前缘和后缘进行Actin细胞骨架的动态重组,其中前缘的肌动蛋白的片状脂质突起与后缘的回缩平行地向前或向后拉动细胞定向运动,同时伴随着粘附位点的改变和RhoA介导的肌动蛋白收缩8,10,11。由于运动细胞前缘受Actin突起的推动,后缘发生收缩,细胞膜发生变形,膜张力发生变化,定向运动依赖于Actin细胞骨架重塑与变形引起的膜张力变化之间的平衡(图1)。
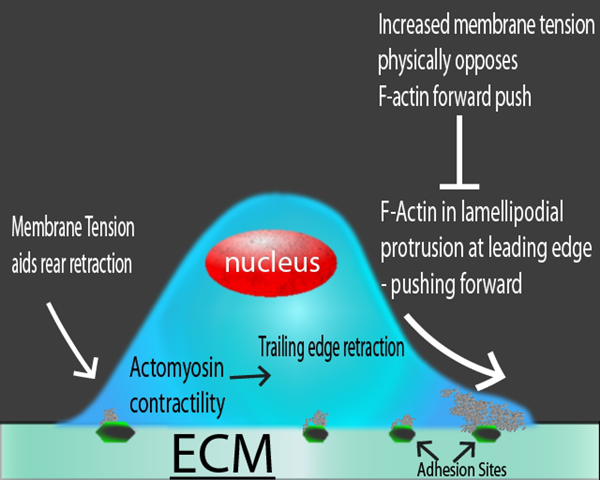
图1:迁移细胞中不同作用力的示意图。在前缘的基于肌动蛋白的突起(即片状脂膜)将细胞向前推动,而膜张力在物理上抵抗这种运动。在后缘,膜张力将帮助Actin介导的收缩。
膜张力和Actin细胞骨架的动态重组是如何相互作用的了?上图中细胞形态变化的运动模型是从早期2D细胞运动实验中获得的,该实验是用鱼角膜细胞的片状脂质体片段或活的完整角膜细胞进行的8,12。该模型假设,运动细胞前缘的聚合Actin网络从内部推动细胞膜,产生与肌动蛋白突起相对的膜张力,在聚合的肌动蛋白网络上快速平衡并施加全局恒定力。
在前缘的中心,高密度的肌动蛋白纤维导致每根丝的膜张力降低,从而使肌动蛋白纤维迅速聚合并驱动前缘向外伸出。随着细胞侧面肌纤维密度减小,每根肌纤维的阻力增加,直到膜张力负荷使肌动蛋白聚合停止,从而形成了细胞的前角。类似地,早期对成纤维细胞的研究也发现,膜张力和突起数呈负相关1。
同时,迁移细胞的后缘有一个可分解的肌动蛋白网络,膜张力的增加会使其解聚加速,从而导致后缘收缩12-14。运动性角膜细胞的活细胞成像研究表明,平面张力(膜本身的张力)和膜细胞骨架附着张力(粘连和肌动球蛋白介导的收缩力)均调节运动细胞的膜张力15,实际上总膜张力由两个因素决定8。Lieber等还证实,随着前缘肌动蛋白聚合的增加,肌纤维向前的推进力也更强从而导致更高的膜张力,反之亦然,在后缘,膜张力与肌球蛋白收缩水平呈负相关,与粘附强度呈正相关15。
最近,在成纤维细胞和成纤维样细胞中的研究进一步阐明了Actin骨架与膜张力之间的相互作用。对成纤维细胞进行的高分辨率显微镜研究显示16,在片状脂质体突起形成早期,当膜贮液充足时,突起的长度就很明显,而膜张力却很低,随着片状脂膜在膜上向外推,膜张力增加,延伸的突起使质膜上的褶皱和曲线平滑,膜贮液耗尽,膜张力迅速增加,同时肌动蛋白细胞骨架重组,导致突起长度缩短16。
在嗜中性粒细胞中,迁移细胞前缘突起的增加与膜张力的增加和除前缘外的其他细胞位置突起的减少是一致的。另一项成纤维细胞研究揭示了膜张力的周期性振荡与片状脂质体突起形态呈负相关17。当膜张力增加时,突起的尺寸(宽度减小)和形状(向上弯曲)都会发生相应变化,并且随着张力的消失,突起会恢复正常的大小,形状和生长活动17。肌动蛋白相关蛋白FBP17(Formin-binding protein)是一种膜弯曲蛋白,是WASP / N-WASP依赖型肌动蛋白成核的活化剂,位于COS-1(成纤维样细胞)细胞迁移的前缘。膜张力通过触发FBP17的膜分离来抑制FBP17的功能,膜张力抑制肌动蛋白的聚合反应从而提供了一个信号传递途径18,19,这表明存在负反馈回路:增加的膜张力通过使肌动蛋白组装分子失活而进一步抑制突起生成8,18,19。其他Actin结合蛋白和MAP蛋白也会参与调节前缘突起的肌动蛋白网络的动态重组20。
摘要
膜张力的功能相关性超出了生物物理范畴,因为膜张力以及其他膜属性,如顺序和电位几乎影响着任何一个重要的生物过程。测量活细胞膜的张力和动态变化是一项非常困难的工作,挑战包括在三维细胞培养中验证在二维细胞培养获得的结果,剖析在不同细胞类型之间膜张力的调节变化,以及不同细胞状态之间膜张力的变化8。
好消息是经过科研工作者们不懈的努力,目前市面上已经有专门用于实时检测活细胞中膜张力变化的械敏感的荧光机探针了9,22,23。艾美捷科技为您推荐Cytoskeleton生产的一种新型的荧光探针,以帮助生物物理学家和细胞生物学家更深入地了解膜张力如何与细胞骨架相互作用以调节基本的细胞功能的。
艾美捷科技为您提供Cytoskeleton的Flipper-TR®活细胞膜张力检测探针 :
| 货号 | 产品名称 | 规格 |
| CY-SC020 | Flipper-TR Membrane Tension Probe | 50 nmol |
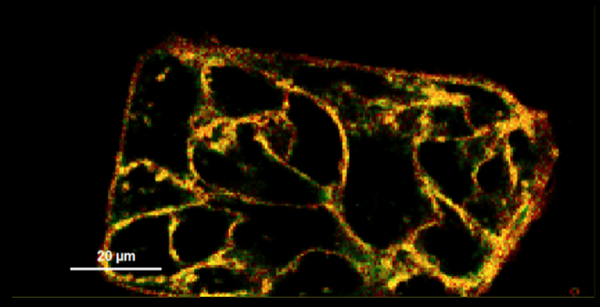
图2:用Flipper-TR膜张力探针(目录号CY-SC020)染色的细胞膜的荧光寿命图。绿色表示中等张力,黄色/橙色/红色表示较高的张力,蓝色表示较低的张力。图片由Colom等提供, 2018.
此外,Cytoskeleton还提供用于F-actin,微管,DNA和溶酶体的活细胞成像探针,以及用于研究细胞中G-actin/F-actin水平和tubulin/微管以及体外相互作用的生化检测试剂盒 。
活细胞成像试剂盒:
| 产品名称 | 货号 |
| SiR-Actin Kit | (Cat. # CY-SC001) |
| SiR-Tubulin Kit | (Cat. # CY-SC002) |
| Cytoskeleton Kit (包括SiR-Actin, SiR-Tubulin,和Verapamil) | (Cat. # CY-SC006) |
| SiR-DNA Kit | (Cat. # CY-SC007) |
| SiR-Lysosome Kit | (Cat. # CY-SC012) |
| SiR700-Actin Kit | (Cat. # CY-SC013) |
| SiR700-Tubulin Kit | (Cat. # CY-SC014) |
| SiR700-DNA Kit | (Cat. # CY-SC015) |
| SiR700-Lysosome Kit | (Cat. # CY-SC016) |
Actin生化试剂盒:
| 产品名称 | 货号 |
| 肌动蛋白结合蛋白 Spin-Down生化检测试剂盒(兔骨骼肌actin) | (Cat. # BK001) |
| 肌动蛋白结合蛋白 Spin-Down生化检测试剂盒(人血小板actin) | (Cat. # BK013) |
| Actin聚合生化检测试剂盒(荧光法:兔骨骼肌actin) | (Cat. # BK003) |
| G-Actin/F-actin In Vivo生化检测试剂盒 | (Cat. # BK037) |
Tubulin生化试剂盒:
| 产品名称 | 货号 |
| Tubulin聚合生化检测试剂盒(比色法) | (Cat. # BK006P) |
| Tubulin聚合生化检测试剂盒(荧光法) | (Cat. # BK011P) |
| 微管结合蛋白 Spin-Down生化检测试剂盒 | (Cat. # BK029) |
| 微管/Tubulin In Vivo生化检测试剂盒 | (Cat. # BK038) |
参考文献:
Raucher D. and Sheetz M.P. 2000. Cell spreading and lamellipodial extension rate is regulated by membrane tension. J. Cell Biol. 148, 127-136.
Keren K. 2011. Cell motility: the integrating role of the plasma membrane. Eur. Biophys. J. 40, 1013-1027.
Diz-Munoz A. et al. 2013. Use the force: Membrane tension as an organizer of cell shape and motility. Trends Cell Biol. 23, 47-53.
Masters T.A. et al. 2013. Plasma membrane tension orchestrates membrane trafficking, cytoskeletal remodeling, and biochemical signaling during phagocytosis. Proc. Natl. Acad. Sci. U.S.A. 110, 11875-11880.
Clark A.G. et al. 2014. Stresses at the cell surface during animal cell morphogenesis. Curr. Biol. 24, R484-R494.
Sens P. and Plastino J. 2015. Membrane tension and cytoskeleton organization in cell motility. J. Phys. Condens. Matter. 27, 273103.
Houk A.R. et al. 2012. Membrane tension maintains cell polarity by confining signals to the leading edge during neutrophil migration. Cell. 148, 175-188.
Pontes B. et al. 2017. Membrane tension: A challenging but universal physical parameter in cell biology. Semin. Cell Dev. Biol. 71, 30-41.
Colom A. et al. 2018. A fluorescent membrane tension probe. Nat. Chem. 10, 1118-1125.
Warner H. et al. 2019. Control of adhesion and protrusion in cell migration by Rho GTPases. Curr. Opin. Cell Biol.56, 64-70.
Lawson C.D. and Ridley A.J. 2018. Rho GTPase signaling complexes in cell migration and invasion. J. Cell Biol. 217, 447-457.
Keren K.et al. 2008. Mechanism of shape determination in motile cells. Nature. 453, 475–480.
Kozlov M.M. and Mogilner A. 2007. Model of polarization and bistability of cell fragments. Biophys. J. 93, 3811–3819.
Ofer N. et al. 2011. Actin disassembly clock determines shape and speed of lamellipodial fragments. Proc. Natl. Acad. Sci. U.S.A. 108, 20394–20399.
Lieber A.D. et al. 2013. Membrane tension in rapidly moving cells is determined by cytoskeletal forces. Curr. Biol.23, 1409-1417.
Gauthier N.C. et al. 2011. Temporary increase in plasma membrane tension coordinates the activation of exocytosis and contraction during cell spreading. Proc. Natl. Acad. Sci. U.S.A. 108, 14467-14472.
Pontes B. et al. 2017. Membrane tension controls adhesion positioning at the leading edge of cells. J. Cell Biol. 216, 2959-2977.
Zegers M.M. and Friedl P. 2015. membrane tension into cytoskeletal action by FBP17. Dev. Cell. 33, 628-630.
Tsujita K. et al. 2015. Feedback regulation between plasma membrane tension and membrane-bending proteins organizes cell polarity during leading edge formation. Nat. Cell Biol. 17, 749-758.
Simon C. et al. 2018. Interplay between membrane tension and the actin cytoskeleton determines shape changes. Phys. Biol. 15, 065004.
Diz-Munoz A. et al. 2016. Membrane tension acts through PLD2 and mTORC2 to limit actin network assembly during neutrophil migration. PLoS Biol. 14, e1002474.
Molin M.D. et al. 2015. Fluorescent flippers for mechanosensitive membrane probes. J. Am. Chem. Soc. 137, 568-571.
Goujon A. et al. 2019. Mechanosensitive fluorescent probes to image membrane tension in mitochondria, endoplasmic reticulum, and lysosomes. J. Am. Chem. Soc. 141, 3380-3384.
Cytoskeleton公司成立于1993年,专注于生物化学和细胞过程研究中的纯化蛋白和便捷试剂盒开发与生产。公司提供药物筛选、信号转导、蛋白质转录后修饰(PTM)、细胞骨架研究相关的系列试剂盒和产品,尤其以细胞骨架相关研究见长,既能满足于样品较少的科学研究,也可以用于小规模筛选研究和高通量大规模筛选研究。此外,公司还提供微管蛋白,肌动蛋白,小G蛋白,GAPs,GEFs等现有产品的药物筛选服务。
作为Cytoskeleton在中国的区域总代理,艾美捷科技有限公司将为中国客户提供最全面的Cytoskeleton产品与服务。

微信扫码在线客服