为了使洗脱蛋白较少污染抗体,也为了更纯净蛋白质的制备和干净的免疫印迹实验,推荐将抗体与珠子交联。下面是一个实验程序举例(几个网站有关于这个程序有很多信息)。目标蛋白应该用温和的洗脱液洗脱,如甘氨酸缓冲液。更详细的缓冲液配方可在缓冲液章节找到,第71页。

裂解物预清除可以帮助减少蛋白质非特异性结合到agarose (琼脂糖)或Sepharose beads (凝胶琼脂糖珠)。用无关抗体或血清预清除,可去除蛋白质与免疫球蛋白的非特异结合。最终实验结果背景降低并且信噪比提高。但是,如果最后蛋白质是由免疫印迹实验检测,预清除未必必要,除非是污染蛋白质对目的蛋白质产生明显干扰。

免疫沉淀是一种纯化蛋白质的方法。将我们感兴趣的一种蛋白质的抗体与细胞提取液孵育,以使抗体和蛋白质在溶液中结合。然后用蛋白A/G 耦合的琼脂糖凝胶,从样品中将抗体/抗原复合物提取出来。这种物理方法可将所需蛋白质从样品中分离出来。然后样品可以通过SDS-PAGE 分离出来进行Western blot 分析。

直接免疫荧光染色时,细胞与直接偶联有荧光染料(如 FITC 标记)的抗体孵育。这种方法的优点在于只需要一步抗体孵育,从而排除了二 抗非特异性结合的可能性。这对细胞内染色特别有用,因为包含二抗的大抗体荧光复合物有可能被困住,造成非特异性结合甚或无法进入细胞,而使一抗检测不到。

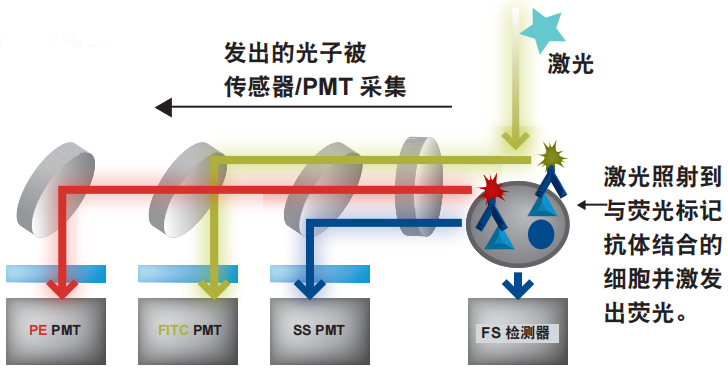
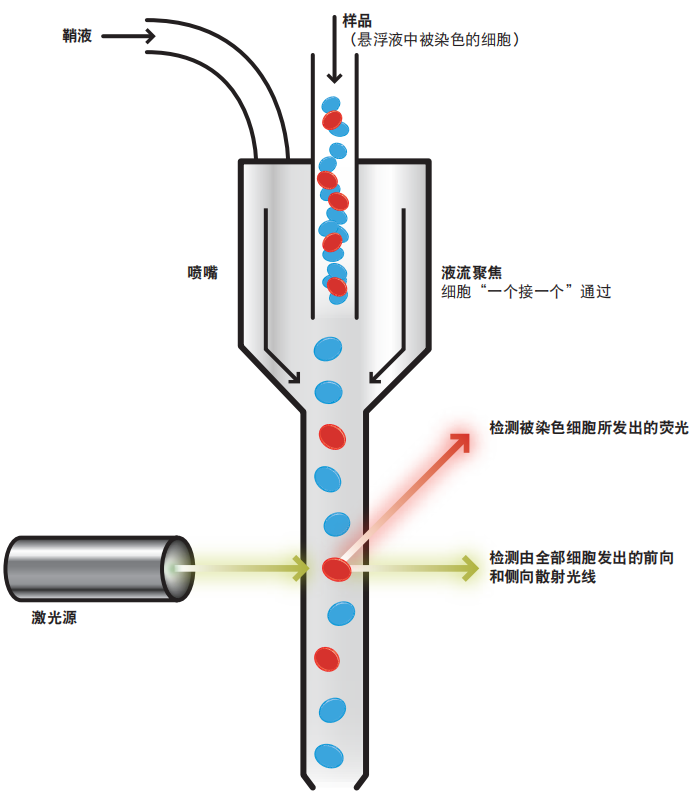
悬浮缓冲液中被染色细胞样品通过流式细胞仪时,由于鞘液的作用,细胞被限制在液流的轴线上,从而能通过一个非常小的喷嘴。这种微小 的“流液束”使细胞一个接一个地通过激光。

用 PBS 或碳酸盐缓冲液稀释抗原至终浓度 20μg/ml。用吸管吸取 50μl 稀释抗原到 PVC 微孔板上,按要求往后进行系列稀释。


用鼠抗体对鼠组织染色是个复杂的过程,因为容易导致背景染色高,而且很难消除。 形成这种背景主要是由于组织染色时二抗与内源性的鼠 IgG,或 B 细胞、浆细胞及巨噬细胞上的 Fc 受体结合造成的。

出于多种考虑,将小组织片段简单浸泡在固定液中便能得到合适的固定,对大多数组织来说可能是唯一的固定模式。然而更快、更均一的固 定方法是将固定液通过管道系统如心主动脉或腹部主动脉灌注到组织中。下面介绍一下用 4% 多聚甲醛固定大鼠大多数器官的操作步骤。

固定就是保持抗原细胞和亚细胞结构固定不动,同时又能使抗体进入到细胞和亚细胞的所有部位。固定和通透方法的选择取决于抗原表位和 抗体本身的灵敏性,有时需要优化。


微信扫码在线客服